En théorie des probabilités, la loi arc sinus est une loi de probabilité à densité…

La loi de Kasha est un principe très important en photochimie. Elle explique comment les molécules émettent de la lumière après l’absorption d’un photon.
Ce phénomène, connu sous le nom de fluorescence ou phosphorescence, se produit toujours à partir de l’état excité de plus basse énergie.
Définition loi de Kasha
La loi de Kasha stipule qu’après l’absorption d’un photon, l’émission radiative se fait depuis l’état excité le plus bas. Cette règle repose sur la rapidité des processus de relaxation vibrationnelle intramoléculaire (RVI), qui sont plus rapides que les processus d’émission photonique.
La fluorescence se produit en nanosecondes, tandis que la phosphorescence peut durer beaucoup plus longtemps.
Cette loi porte le nom de Michael Kasha, un spectroscopiste américain. Kasha a formulé cette règle après avoir observé des comportements spécifiques des molécules en état excité.
Ses travaux ont profondément influencé la compréhension moderne de la photochimie et de la spectroscopie. Les contributions de Kasha restent fondamentales pour les recherches en chimie et en physique.
Quel est le principe de la loi de Kasha ?
La loi de Kasha stipule que l’émission radiative se produit toujours depuis l’état excité de plus basse énergie. Après l’absorption d’un photon, une molécule atteint un état excité.
Ensuite, elle émet de la lumière en revenant à son état fondamental. Ce processus se réalise rapidement et efficacement.
Processus de relaxation vibrationnelle intramoléculaire (RVI)
La relaxation vibrationnelle intramoléculaire (RVI) est cruciale dans ce contexte. Elle permet à l’énergie absorbée de se dissiper rapidement entre les niveaux excités.
Ce phénomène se produit en quelques femtosecondes. Ainsi, la molécule atteint rapidement l’état excité le plus bas avant d’émettre de la lumière.
Différences entre fluorescence et phosphorescence
La fluorescence et la phosphorescence diffèrent par leur durée et leurs mécanismes. La fluorescence se produit en nanosecondes. Elle résulte de transitions autorisées par le spin.
En revanche, la phosphorescence peut durer beaucoup plus longtemps, parfois plusieurs minutes. Elle résulte de transitions interdites par le spin.
Ces différences influencent les applications pratiques de chaque processus.
Mécanismes sous-jacents
Schématisation de la loi de Kasha
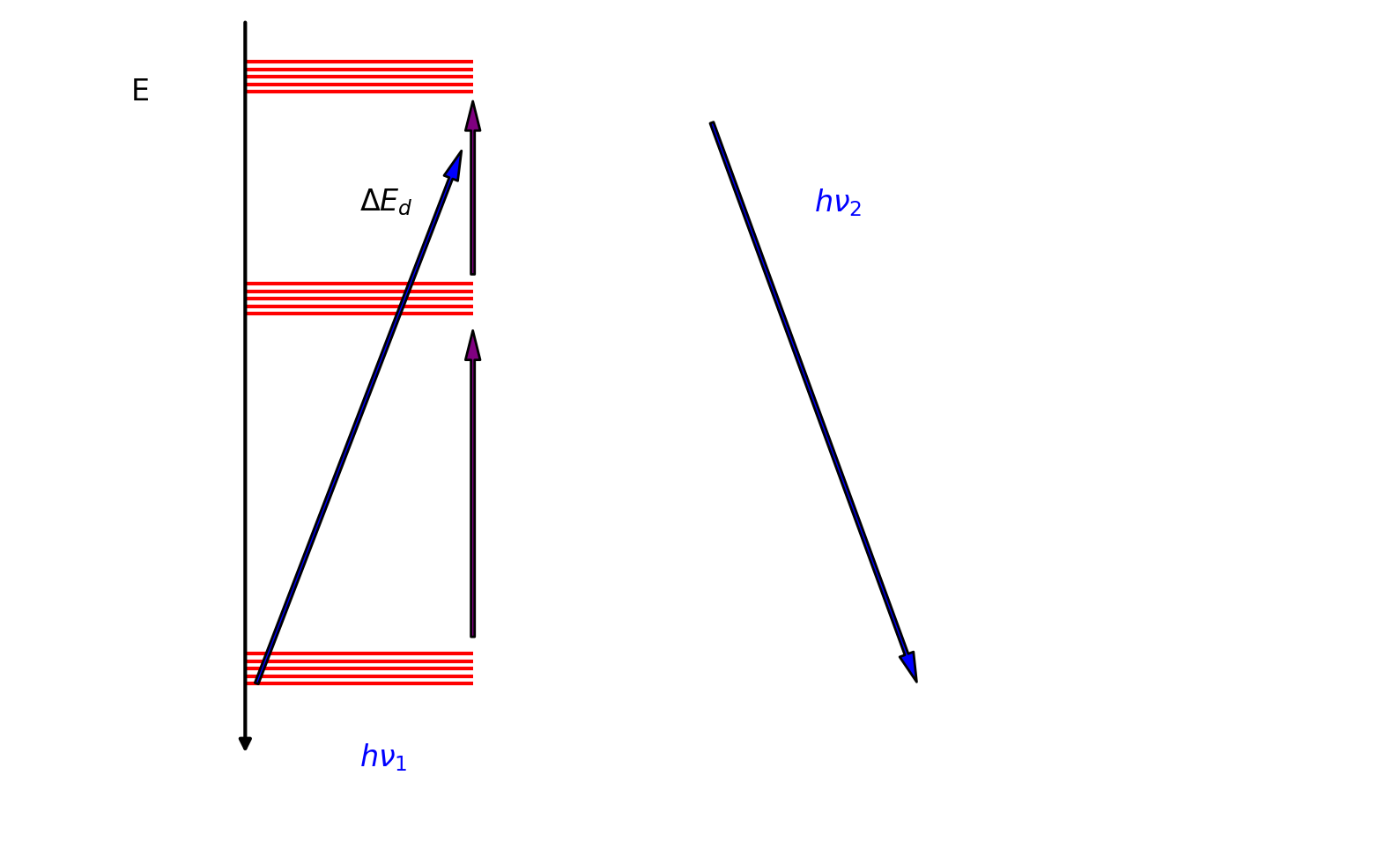
La loi de Kasha peut être schématisée simplement. Un photon d’énergie excite une molécule. Celle-ci passe à un état excité.
Ensuite, elle relaxe rapidement à l’état excité le plus bas par relaxation vibrationnelle. Enfin, elle émet un photon pour revenir à l’état fondamental.
Facteurs de Franck-Condon et recouvrement vibrationnel
Les facteurs de Franck-Condon jouent un rôle crucial dans les transitions électroniques. Ils déterminent la probabilité des transitions en fonction du recouvrement vibrationnel.
Un meilleur recouvrement entraîne une plus grande probabilité de transition. Cependant, la loi de Kasha s’applique indépendamment de ce recouvrement.
Intersections coniques et conversion interne
Les intersections coniques sont des points où deux surfaces d’énergie potentielle se croisent. Elles permettent des transferts énergétiques rapides entre états électroniques.
Ce processus, appelé conversion interne, se produit généralement entre états de même multiplicité de spin. Les intersections coniques facilitent une désactivation rapide vers l’état excité le plus bas, favorisant ainsi l’émission radiative conforme à la loi de Kasha.
Applications et implications
Importance en photochimie et spectroscopie
La loi de Kasha est cruciale en photochimie et en spectroscopie. Elle aide à comprendre les comportements des molécules après l’absorption de lumière.
En photochimie, elle permet de prédire l’efficacité des réactions lumineuses. En spectroscopie, elle facilite l’analyse des émissions lumineuses des molécules.
Rôles des états excités électroniques
Les états excités électroniques jouent un rôle clé dans la loi de Kasha. Après l’absorption de lumière, une molécule atteint un état excité. La conversion interne amène rapidement la molécule à l’état excité le plus bas.
Ensuite, l’émission radiative se produit. Ce processus est essentiel pour des technologies comme les LED, les lasers et les cellules photovoltaïques. Il influence également la conception de nouveaux matériaux photoactifs.
Exceptions à la loi de Kasha
Cas de fluorescence double
La fluorescence double constitue une exception notable à la loi de Kasha. Certaines molécules peuvent émettre de la lumière à partir de plusieurs états excités.
Cette fluorescence multiple peut se produire malgré la règle générale.
Exemples spécifiques : azulène, aminobenzonitriles, phénylpyrrole
L’azulène est un exemple classique de fluorescence double. Il émet de la lumière depuis les états S1 et S2. Les aminobenzonitriles montrent également une fluorescence double. Ils possèdent deux minima distincts sur la surface d’énergie de l’état S1.
Le phénylpyrrole présente un comportement similaire. Ces exceptions illustrent la complexité des processus photochimiques et les limites de la loi de Kasha.
Techniques expérimentales et études de cas
Spectroscopie ultrarapide
La spectroscopie ultrarapide est essentielle pour étudier les processus photochimiques. Elle capture des événements se produisant en quelques femtosecondes.
Cette technique permet d’observer les étapes initiales après l’absorption de lumière.
Études des processus initiaux post-absorption de lumière
Les processus initiaux après l’absorption de lumière déterminent le comportement des molécules excitées. Comprendre ces étapes est crucial pour la photochimie.
La spectroscopie ultrarapide révèle des détails sur ces transitions rapides et complexes.
Exemples de réactions photochimiques ultrarapides
Des réactions photochimiques ultrarapides comme les transferts de charge et les conversions internes montrent l’importance de ces processus.
Par exemple, les réactions dans des systèmes biologiques ou des matériaux photovoltaïques dépendent de ces dynamiques rapides.
Analyser ces réactions permet de concevoir des dispositifs plus efficaces et d’améliorer notre compréhension des mécanismes photochimiques.
Quels sont les avantages de la loi de Kasha ?
La loi de Kasha présente plusieurs avantages dans les domaines de la photochimie et de la spectroscopie. Voici quelques-uns des principaux avantages :
- Prédiction des Émissions : La loi de Kasha permet de prédire que l’émission radiative se fera à partir de l’état excité de plus basse énergie. Cela simplifie l’analyse des spectres de fluorescence et de phosphorescence.
- Modélisation Simplifiée : Grâce à cette loi, les modèles théoriques et les simulations de comportements moléculaires après absorption de photons deviennent plus simples et plus précis.
- Compréhension des Relaxations : La loi met en lumière l’importance des processus de relaxation vibrationnelle intramoléculaire (RVI), permettant une meilleure compréhension de la dissipation d’énergie au sein des molécules.
- Applications Technologiques : Elle est essentielle dans la conception et l’optimisation des dispositifs optiques tels que les LED, les lasers et les cellules photovoltaïques, en assurant que les matériaux utilisés aient les propriétés lumineuses souhaitées.
- Innovation en Matériaux : Les chercheurs peuvent concevoir de nouveaux matériaux photoactifs en s’appuyant sur les principes de la loi de Kasha, ce qui facilite le développement de matériaux aux propriétés optiques spécifiques.
- Interprétation des Spectres : En spectroscopie, la loi de Kasha aide à interpréter les spectres d’émission des composés chimiques, ce qui est crucial pour l’identification et l’analyse des substances.
- Fiabilité des Données : Les expériences basées sur la loi de Kasha produisent des données plus fiables, car les attentes concernant les états d’émission sont claires et bien définies.
- Facilite la R&D : La loi de Kasha sert de guide pour les chercheurs en développant des réactions photochimiques efficaces, ce qui est vital pour les avancées en chimie, biologie et science des matériaux.
Conclusion
La loi de Kasha stipule que l’émission radiative se produit depuis l’état excité le plus bas. Ce principe repose sur des processus de relaxation vibrationnelle intramoléculaire rapides.
Les exceptions, comme la fluorescence double, illustrent la complexité des interactions photochimiques. La spectroscopie ultrarapide permet d’étudier les étapes initiales après l’absorption de lumière.
La loi de Kasha est fondamentale en photochimie et en spectroscopie. Elle aide à comprendre les mécanismes d’émission de lumière des molécules.
Ces connaissances sont cruciales pour le développement de nouvelles technologies, comme les LED et les cellules photovoltaïques.
En fin de compte, la loi de Kasha reste un pilier pour les chercheurs en photochimie, offrant des insights précieux sur les dynamiques moléculaires post-excitation.
Références et sources utilisées
-
- Kasha, M. (1950). « Characterization of Electronic Transitions in Complex Molecules. » Discuss. Faraday Soc., 9, 14-19. DOI:10.1039/DF9500900014.
- McClure, D.S. (1955). « Triplet-Singlet Transitions in Organic Molecules. Phosphorescence and the Mechanism of Electronic Energy Transfer. » J. Chem. Phys., 23, 1837-1845. DOI:10.1063/1.1740688.
- Turro, N.J. (1978). Modern Molecular Photochemistry. Benjamin/Cummings.
- Birks, J.B. (1970). Photophysics of Aromatic Molecules. Wiley-Interscience.
- Herzberg, G. (1945). Molecular Spectra and Molecular Structure: II. Infrared and Raman Spectra of Polyatomic Molecules. Van Nostrand.
- Callis, P.R. (1983). « Electrostatic Influences on the Absorption and Emission of Organic Dyes in Solution. » J. Chem. Phys., 78, 4233-4245. DOI:10.1063/1.444417.
- Fleming, G.R. (1986). Chemical Applications of Ultrafast Spectroscopy. Oxford University Press.
- Lakowicz, J.R. (2006). Principles of Fluorescence Spectroscopy. Springer.
- Mukamel, S. (1995). Principles of Nonlinear Optical Spectroscopy. Oxford University Press.
- Valeur, B., & Berberan-Santos, M.N. (2012). Molecular Fluorescence: Principles and Applications. Wiley-VCH.




Commentaires